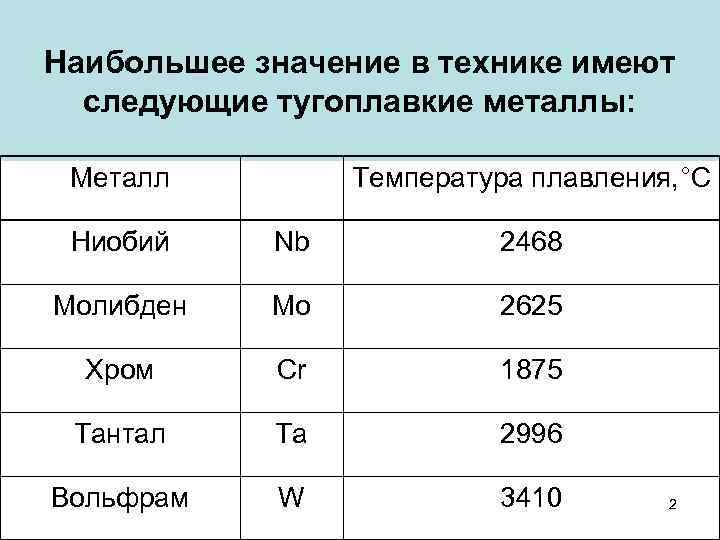
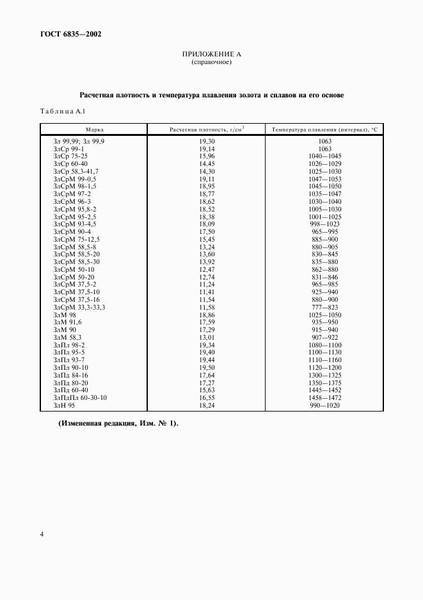
Сплавы на основе платины
Металл имеет магнитные свойства, а сплав на его основе с кобальтом применяется для изготовления мощных постоянных магнитов. Аноды, основанные на платине, применяются в производстве трубопроводов.
Соединения платины применяются в медицине и являются составной частью химиотерапии для лечения некоторых видов заболеваний.
Формирование сплавов металла относится к металлургической отрасли. Соединения на основе платины широко используются в ювелирном производстве преимущественно способом литья по выплавляемым моделям.

При формировании соединений с другими материалами учитывается удельная теплота плавления каждого компонента состава. Сплавы на основе платины широко применяются для изготовления украшений, благодаря таким свойствам:
- высокому качеству материала;
- красивому внешнему виду;
- устойчивости к воздействию внешних факторов и коррозии;
- легкости обработки;
- сочетанию с бриллиантами.
Наиболее популярными являются соединения с содержанием примесей других компонентов 1–5%. Сплав, в состав которого входит 5% меди, имеет красивый внешний вид и применяется в основном для изготовления колец методом штамповки.
Низкие литейные свойства и высокая температура плавления усложняют его применения для другой технологии производства. Наличие в составе материала галлия (1–10% массы), марганца или кобальта (0,1–5%) и основного драгоценного компонента (84–96%) позволяет использовать соединение для литья мелких деталей изделий.
Снижение концентрации галлия и кобальта влечет повышение температуры плавления состава. Наличие большего количества лигатурных добавок влияет на цвет и блеск состава.
Источник
Состав сплава ЦАМ
Это разновидность цинкового сплава, основными легирующими элементами которого является алюминий и медь. Сама аббревиатура ЦАМ расшифровывается как цинк-алюминий-медь. Цифры, указанные после названия сплава, обозначают процентное содержание металлов. Так обозначение ЦАМ 4-1 говорит, что сплав включает в себя пр имерно 4% алюминия, 1% меди и 95% цинка. Также ЦАМ всегда содержат в своем составе небольшое количество (до 0,1%) магния.
Цинк представляет собой пластичный металл серебристого цвета и белого оттенка. Достаточно хрупок. Отличается пониженной температурой плавления, высокой жидкотекучестью и низкой стоимостью. Является основой для ЦАМ.
Алюминий сокращает растворимость железа в сплаве, что благоприятно воздействует на механические и литейные характеристики ЦАМа. Помимо этого, алюминий уменьшает влияние зональной ликвации. Способствует измельчению зерна.
Медь вводят в сплав с целью увеличения его прочностных характеристик. Один процент меди повышает значение твердости ЦАМ примерно на 7%. Обратной стороной данного легирования является ухудшение коррозионностойких и пластичных свойств сплава.
Магний – компонент, отвечающий за сдерживание ЦАМом зарождения очагов коррозии, включая самую худшую ее разновидность – мелкозернистую. Также он замедляет процессы старения в сплаве. Чрезмерное легирование ЦАМа магнием (свыше 0,1%) приводит к ухудшению пластичности, прочности и появлению признаков красноломкости.
Помимо основных элементов сплав включает в себя компоненты, отрицательно влияющие на его свойства – вредные примеси. Причиной этому служит несовершенство технологии выплавки и чистота применяемой шихты. Наиболее часто встречаемые примеси – это:
- Олово (до 0,001%).
- Свинец (до 0,007%).
- Кадмий (до 0,003%).
- Железо (до 0,1%).
Попадание данных металлов с ЦАМ приводят к снижению механических характеристик, жидкотекучести и повышает склонность к образованию трещин.
Металлургия предлагает свыше 25 разновидностей ЦАМа, но наибольшее распространение среди них получили такие марки как:
- ЦАМ 4-1 ГОСТ 19424-97.
- ЦАМ 4-3 ГОСТ 19424-97.
- ЦАМ 9-1,5 ГОСТ 21438-95.
- ЦАМ 10-5 ГОСТ 24438-95.
Физические свойства
Плотность ЦАМ равна 6700 кг\м3. Температура плавления колеблется в пределах 380-387 градусов в зависимости от марки сплава. Кипеть ЦАМ начинает при температуре в 710 С
Цинковый сплав хорошо проводит тепло. Коэффициент теплопроводности составляет 110 ВТ\м*К. Имеет незначительный коэффициент линейного расширения. При повышении температуры на 20 градусов длина бруска из ЦАМа увеличивается на 27,7 мкм.
Механические свойства
Прочность ЦАМ по своему значению сравнима с прочностными характеристиками стали 20. Временное сопротивление разрыву равно 245 МПа. Деформироваться начинает при нагрузке в 120 МПа. Твердость сплавов по шкале Бринелля составляет 95-100 единиц.
Пластичные свойства сильно зависят от количественного содержания легирующих элементов в составе. Исходя из их содержания относительное удлинение на растяжение может колебаться от 0,4 до 1,0%.
Химические свойства
Сплавы ЦАМ отличаются хорошей сопротивляемостью к образованию коррозии. Хотя обязательным условием при этом должно быть предварительное нанесение на их поверхность гальванических покрытий. Активно взаимодействует с большинством кислот и щелочей.
ЦАМы не вступают в химические реакции с такими химическими элементами как азот, углерод, водород, бор и кремний. Инертен к аммиачной среде при температуре до 480 градусов.
Технологические свойства
В зависимости от технологического назначения ЦАМ делятся на следующие категории:
- Литейные сплавы. Сюда в первую очередь относят ЦАМ 4-1 и 4-3. Данные марки отличаются повышенными литейными свойствами. Значение их жидкотекучести и усадки позволяет получать тонкостенные (до 0,5 мм) отливки сложной формы. Основной способ изготовления таких заготовок – это литье под давлением.
- Антифрикционные сплавы (ЦАМ 9-1,5 и 10-5) выделяются пониженным коэффициентом терния, чье значение достигает порядка 0,007 единиц.
- Деформируемые сплавы ЦАМ обладают повышенной пластичностью и пониженной красноломкостью, что позволяет их обрабатывать давлением. Помимо этого, они также хорошо поддаются обработке резанием.
ЦАМы относятся к третьей группе свариваемости. Получить качественный сварной шов для данного сплава весьма проблематично Одним из таких вероятных способов является использование аргонодуговой сварки с медной или алюминиевой присадкой при постоянном токе.
Также одним из достоинств цинковых сплавов является возможность доводки поверхности. ЦАМы хорошо подаются полированию и не отличаются склонностью к образованию зазубрин и заусенцев.

Исторический ракурс
Согласно историческим данным, первый медный сплав появился к 7 тыс. до н.э. Позже в качестве добавки стало использоваться олово. В это время, именуемое бронзовым веком, из такого материала изготавливалось оружие, зеркала, посуда и украшения.
Технология производства менялась. Появились добавки в виде мышьяка, свинца, цинка и железа. Все зависело от требований, предъявляемых к предмету. Материал для украшений нуждался в особом подходе. Состав сплава состоял из меди, олова и свинца.
Начиная с 8 в. до н. э. в Малой Азии была разработана технология получения латуни. В это время еще не научились добывать чистый цинк. Поэтому в качестве сырья использовалась его руда. С течением времени производство медных сплавов постоянно расширялось и до сих пор находится на первых местах.
Как происходит
 Плавление всех металлов происходит примерно одинаково — при помощи внешнего или внутреннего нагревания. Первый осуществляется в термической печи, для второго используют резистивный нагрев при пропускании электрического тока или индукционный нагрев в высокочастотном электромагнитном поле. Оба варианта воздействуют на металл примерно одинаково.
Плавление всех металлов происходит примерно одинаково — при помощи внешнего или внутреннего нагревания. Первый осуществляется в термической печи, для второго используют резистивный нагрев при пропускании электрического тока или индукционный нагрев в высокочастотном электромагнитном поле. Оба варианта воздействуют на металл примерно одинаково.
При увеличении температуры увеличивается и амплитуда тепловых колебаний молекул, возникают структурные дефекты решетки, выражающиеся в росте дислокаций, перескоке атомов и других нарушениях. Это сопровождается разрывом межатомных связей и требует определенного количества энергии. В это же время происходит образование квази-жидкого слоя на поверхности тела. Период разрушения решетки и накопления дефектов называется плавлением.
Как происходит
 Плавление всех металлов происходит примерно одинаково — при помощи внешнего или внутреннего нагревания. Первый осуществляется в термической печи, для второго используют резистивный нагрев при пропускании электрического тока или индукционный нагрев в высокочастотном электромагнитном поле. Оба варианта воздействуют на металл примерно одинаково.
Плавление всех металлов происходит примерно одинаково — при помощи внешнего или внутреннего нагревания. Первый осуществляется в термической печи, для второго используют резистивный нагрев при пропускании электрического тока или индукционный нагрев в высокочастотном электромагнитном поле. Оба варианта воздействуют на металл примерно одинаково.
При увеличении температуры увеличивается и амплитуда тепловых колебаний молекул, возникают структурные дефекты решетки, выражающиеся в росте дислокаций, перескоке атомов и других нарушениях. Это сопровождается разрывом межатомных связей и требует определенного количества энергии. В это же время происходит образование квази-жидкого слоя на поверхности тела. Период разрушения решетки и накопления дефектов называется плавлением.
Физические и химические свойства сплавов
Химический состав и механические свойства медных сплавов обеспечивают им не только прочность, но и хорошую электро- и теплопроводность. Особенно это относится к латуни.
Все медные сплавы характеризуются хорошими антифрикционными свойствами. Отдельно стоит отметить бронзу.
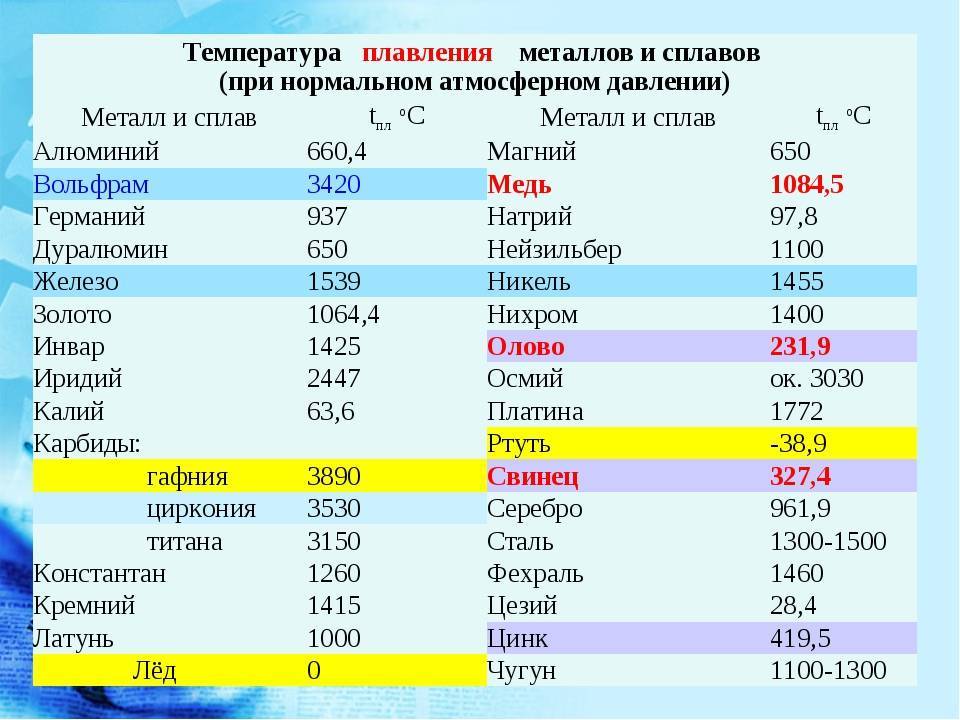
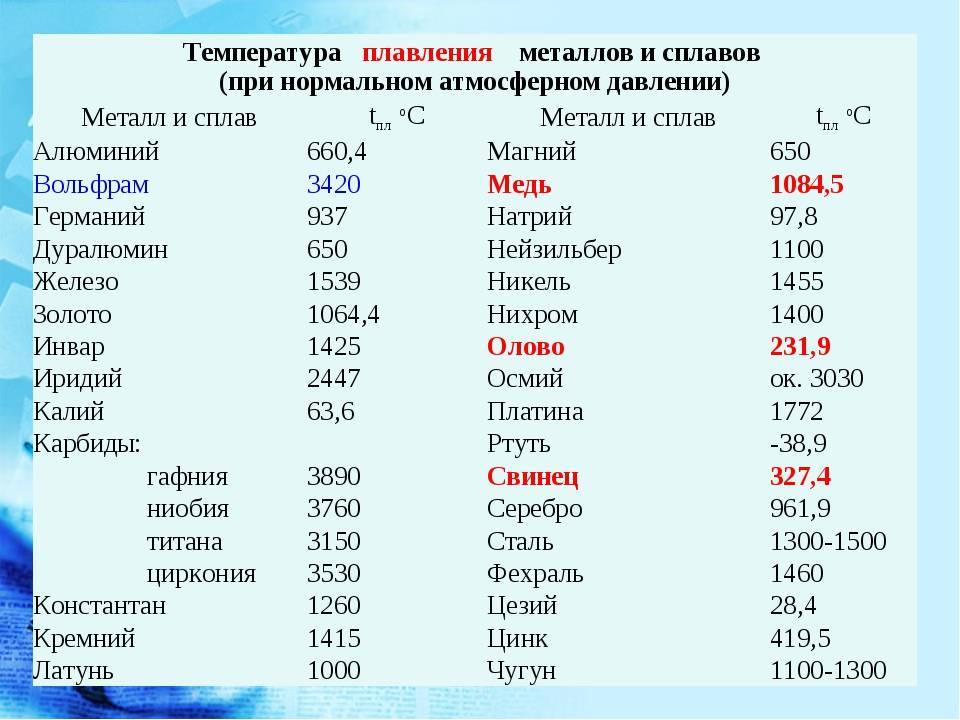
Температура плавления меди без добавок составляет 1083 градуса. В зависимости от количества добавления цинка и олова, этот показатель меняется. Величина температуры плавления латуни составляет 900–1050 градусов, а бронзы — 930–1140 градусов.
Коррозионные свойства медных сплавов отличаются стойкостью. Связано это с тем, что медь не активный элемент. Особенно не корродируют полированные поверхности.
Коррозионная стойкость медных соединений проявляется в пресной воде и ухудшается в присутствии кислоты, которая препятствует образованию защитной оболочки.
Цвет:
Цвет у большинства металлов примерно одинаковый — светло-серый, иногда с голубоватым оттенком. Золото, медь и цезий соответственно жёлтого, красного и светло-жёлтого цвета.
Металлы подразделяются на цветные и черные.
Чёрные металлы – железо и сплавы на его основе (стали, ферросплавы, чугуны). К чёрным металлам также зачастую относят марганец и, иногда, – хром и ванадий.
Цветные металлы — это особый класс нержавеющих металлов и сплавов, в составе которых нет железа. Металлы называются цветными, потому что каждый из них имеет определенный окрас. К цветным металлам относятся медь, молибден, свинец, цинк, олово, никель, кадмий, кобальт, алюминий, титан, магний, висмут, вольфрам, ртуть, золото, платину, серебро, палладий, родий, рутений, осмий, иридий.
Примечание: Фото https://www.pexels.com, https://pixabay.com
Найти что-нибудь еще?
карта сайта
Коэффициент востребованности
960
Прочность металлов
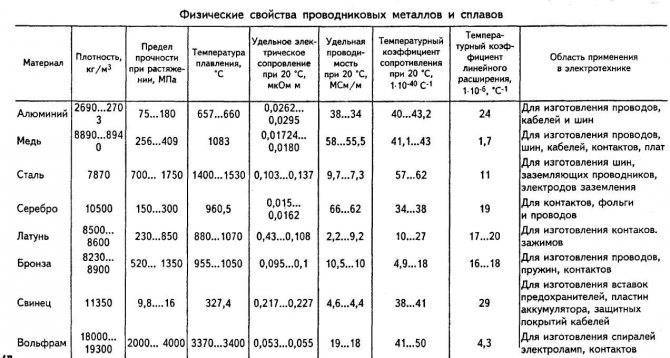
 Помимо способности перехода из твердого в жидкое состояние, одним из важных свойств материала является его прочность — возможность твердого тела сопротивлению разрушению и необратимым изменениям формы. Основным показателем прочности считается сопротивление возникающее при разрыве заготовки, предварительно отожженной. Понятие прочности не применимо к ртути, поскольку она находится в жидком состоянии. Обозначение прочности принято в МПа — Мега Паскалях.
Помимо способности перехода из твердого в жидкое состояние, одним из важных свойств материала является его прочность — возможность твердого тела сопротивлению разрушению и необратимым изменениям формы. Основным показателем прочности считается сопротивление возникающее при разрыве заготовки, предварительно отожженной. Понятие прочности не применимо к ртути, поскольку она находится в жидком состоянии. Обозначение прочности принято в МПа — Мега Паскалях.
Существуют следующие группы прочности металлов:
- Непрочные. Их сопротивление не превышает 50МПа. К ним относят олово, свинец, мягкощелочные металлы
- Прочные, 50−500МПа. Медь, алюминий, железо, титан. Материалы этой группы являются основой многих конструкционных сплавов.
- Высокопрочные, свыше 500МПа. Например, молибден и вольфрам.
Таблица прочности металлов
| Металл | Сопротивление, МПа |
|---|---|
| Медь | 200−250 |
| Серебро | 150 |
| Олово | 27 |
| Золото | 120 |
| Свинец | 18 |
| Цинк | 120−140 |
| Магний | 120−200 |
| Железо | 200−300 |
| Алюминий | 120 |
| Титан | 580 |
Наиболее распространенные в быту сплавы
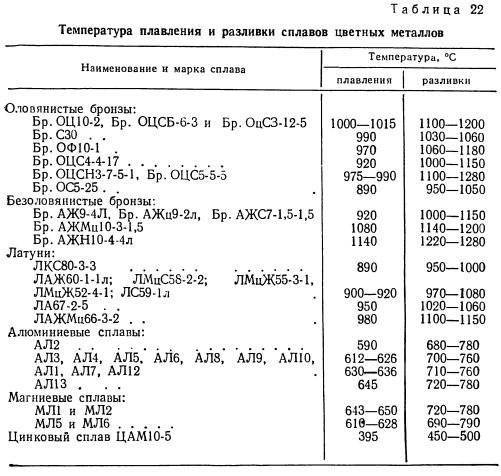
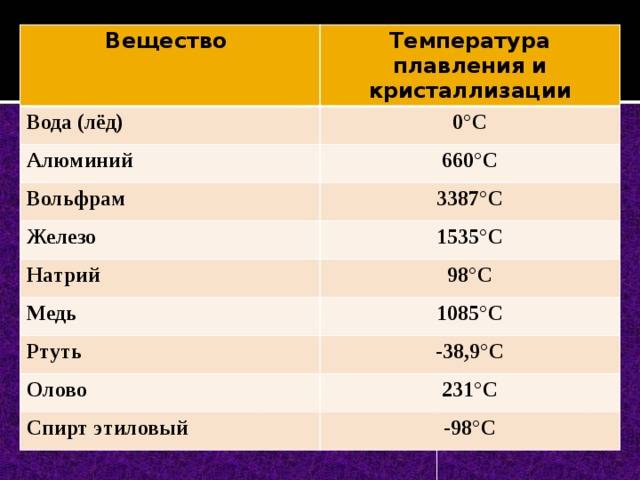
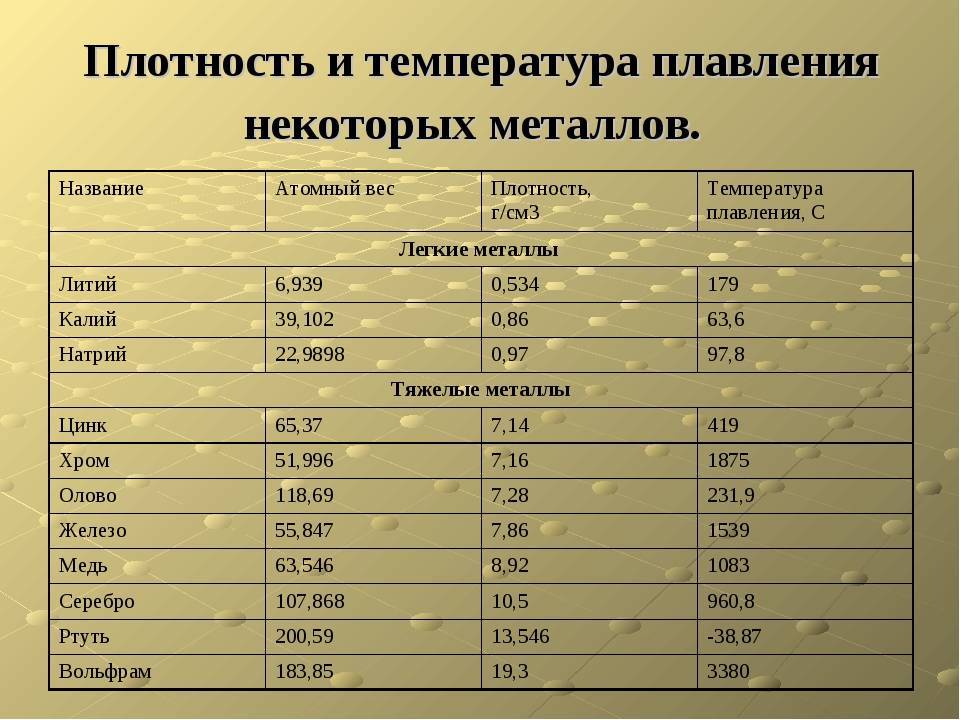
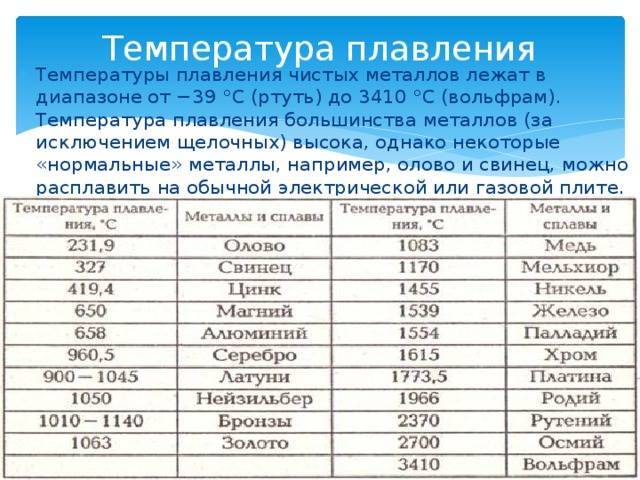
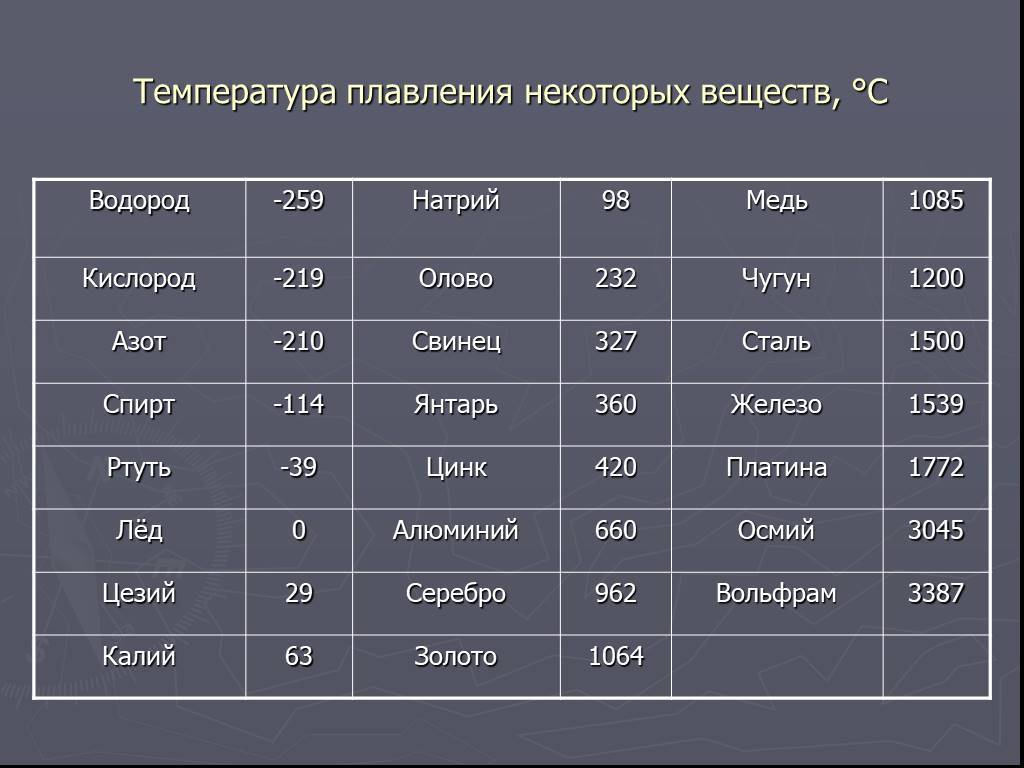
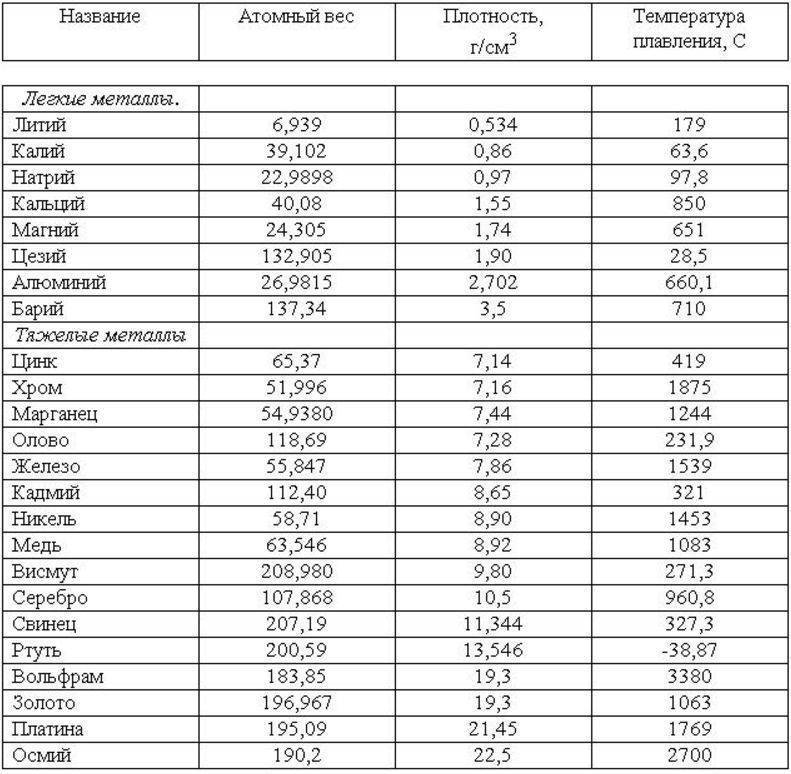
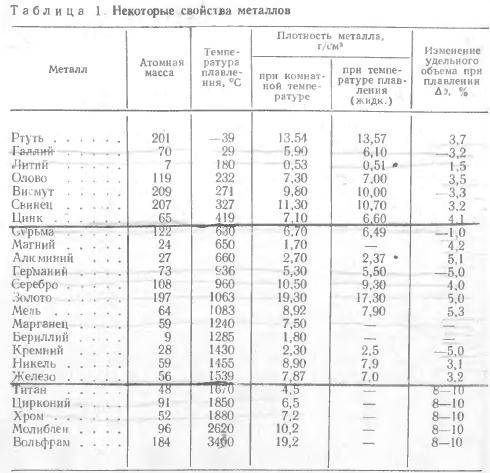
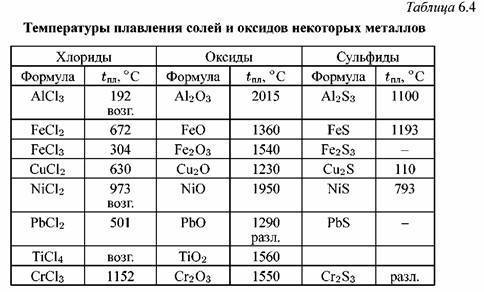
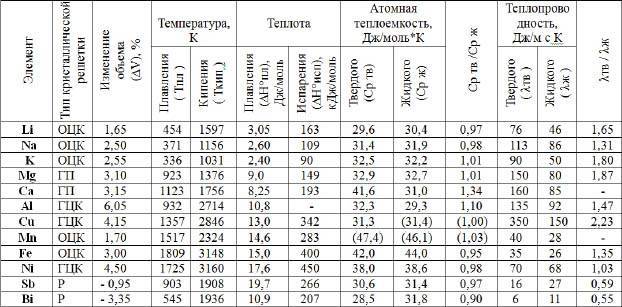
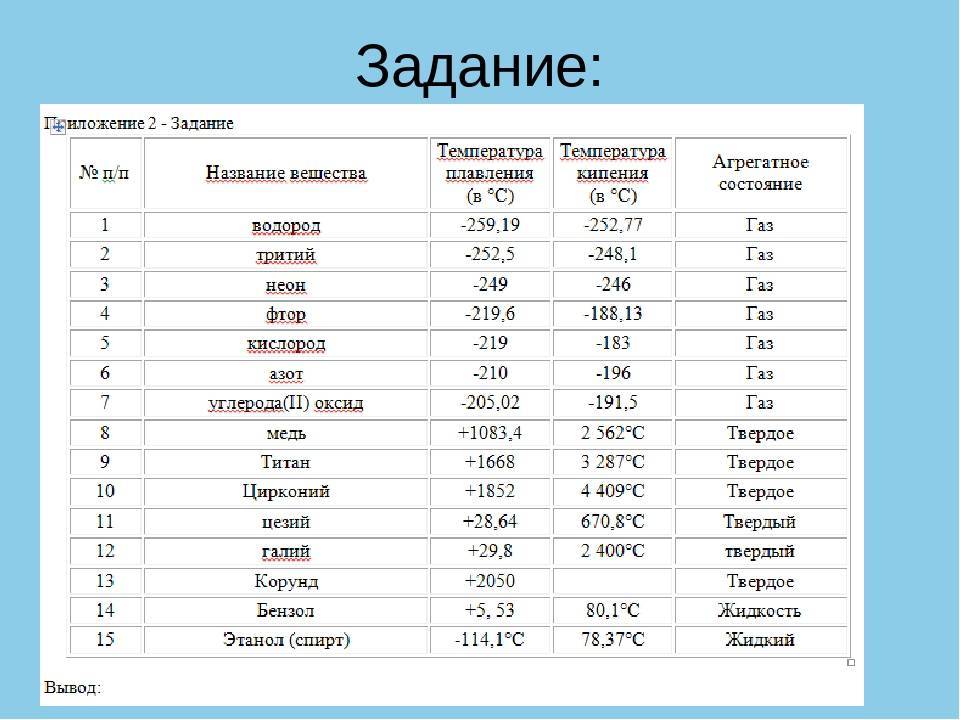
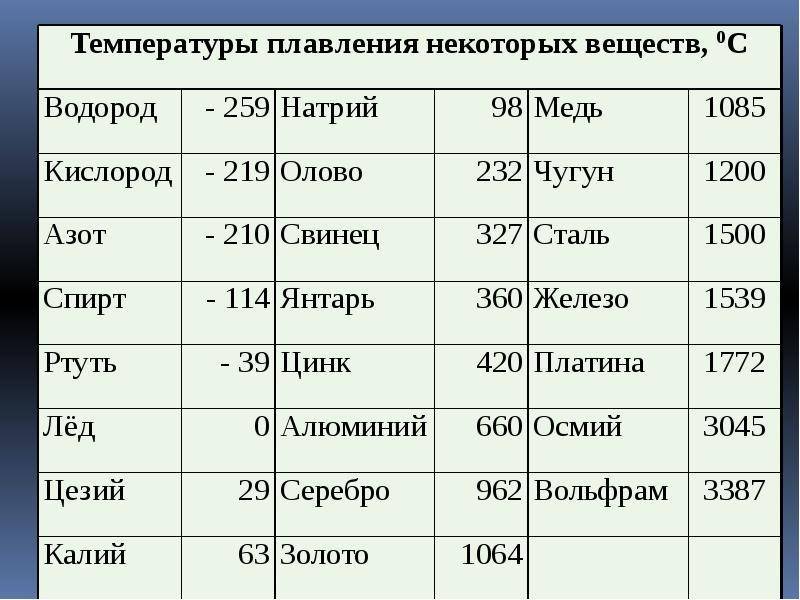
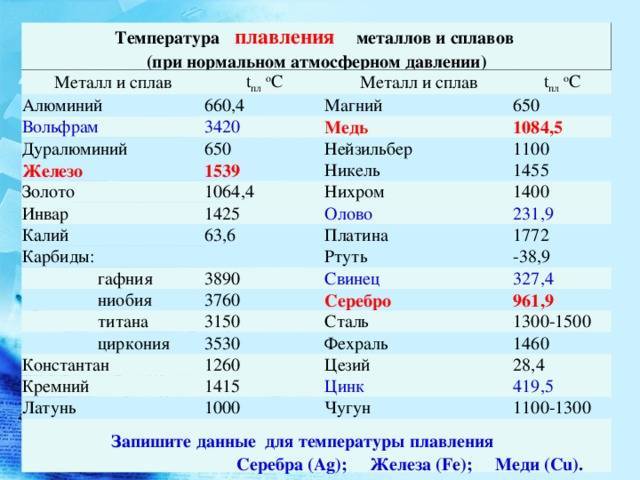
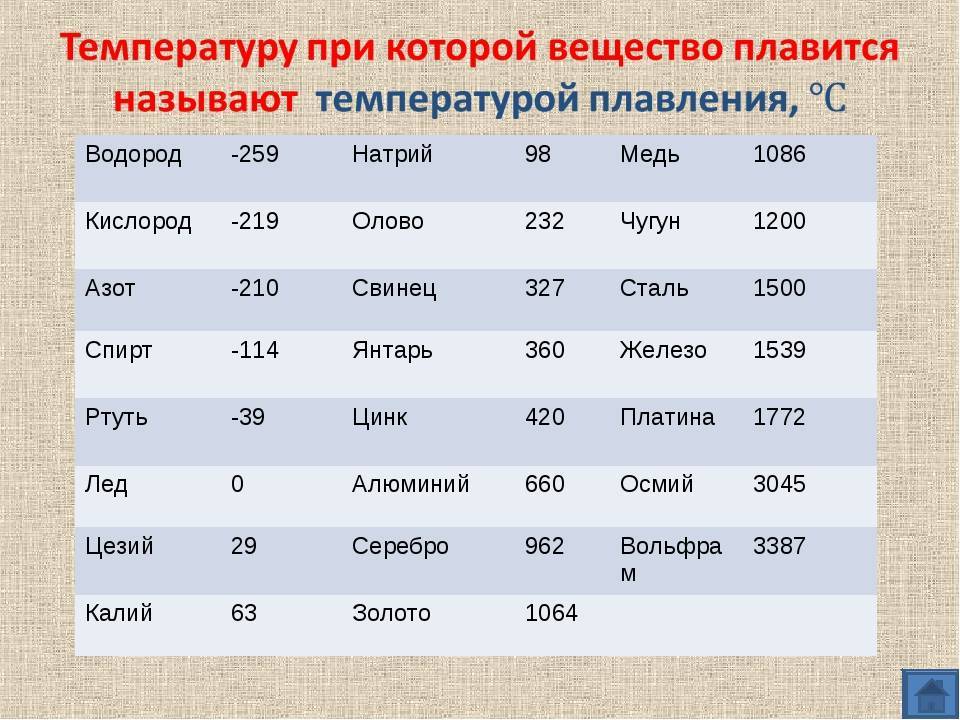
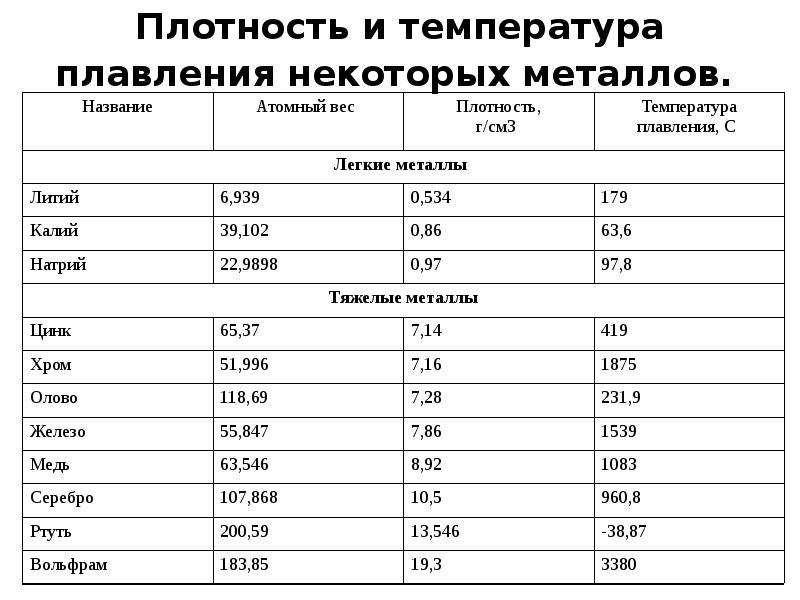
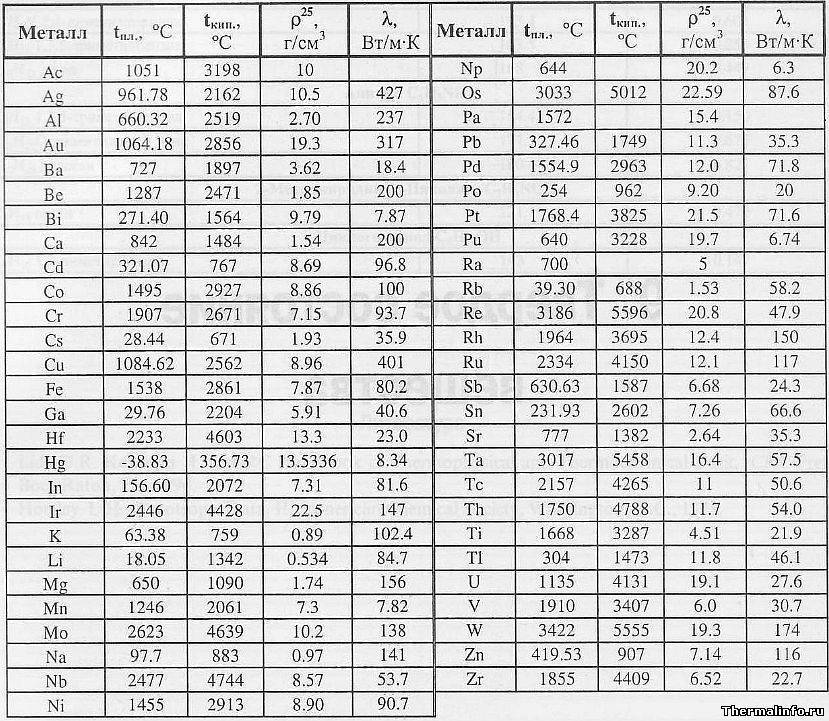
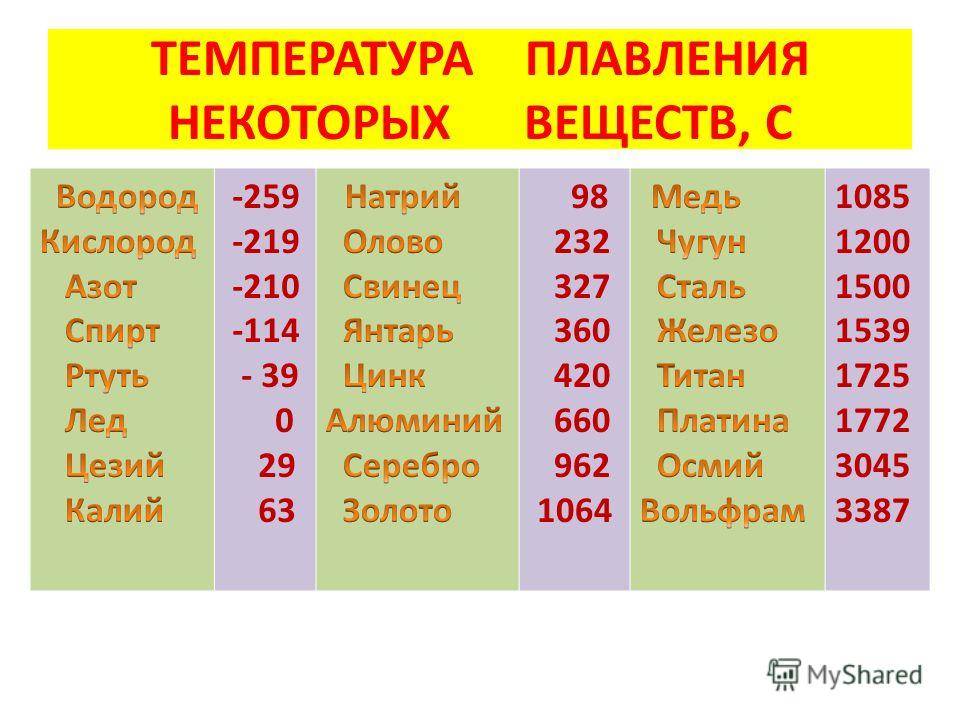
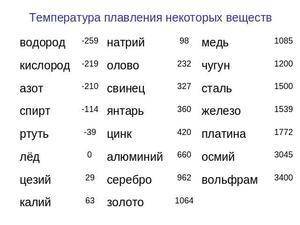
 Как видно из таблицы, точки плавления элементов сильно разнятся даже у часто встречающихся в быту материалов.
Как видно из таблицы, точки плавления элементов сильно разнятся даже у часто встречающихся в быту материалов.
Так, минимальная температура плавления у ртути -38,9 °C, поэтому в условиях комнатной температуры она уже в жидком состоянии. Именно этим объясняется то, что бытовые термометры имеют нижнюю отметку в -39 градусов Цельсия: ниже этого показателя ртуть переходит в твердое состояние.
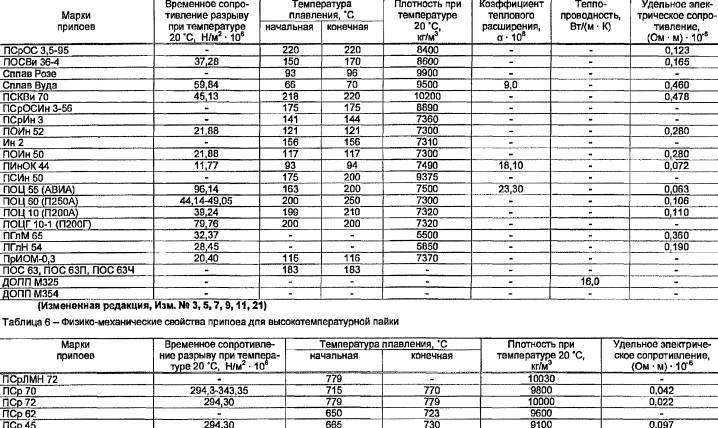
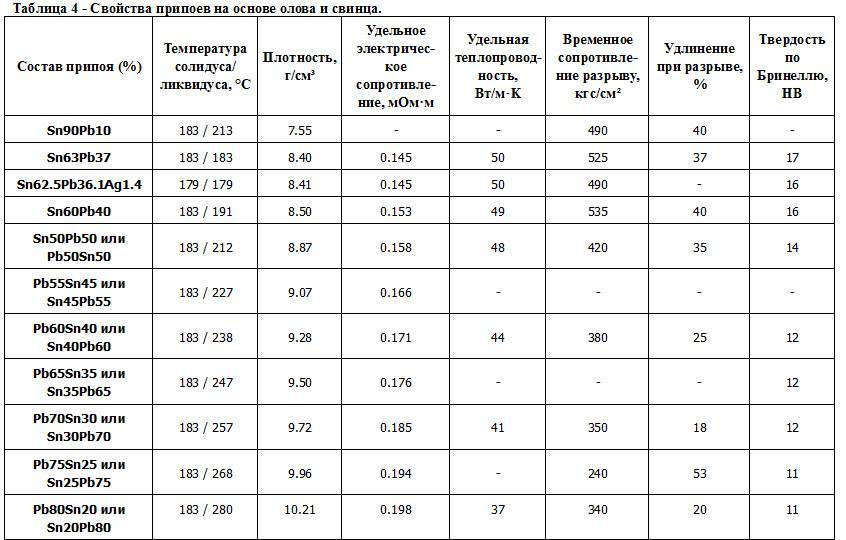
Припои, наиболее распространенные в бытовом применении, имеют в своем составе значительный процент содержания олова, имеющего точку плавления 231.9 °C, поэтому большая часть припоев плавится при рабочей температуре паяльника 250−400°C.
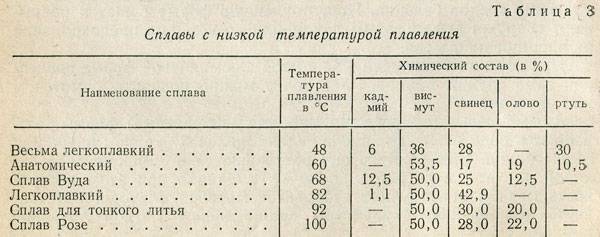
Помимо этого, существуют легкоплавкие припои с более низкой границей расплава, до 30 °C и применяются тогда, когда опасен перегрев спаиваемых материалов. Для этих целей существуют припои с висмутом, и плавка данных материалов лежит в интервале от 29,7 — 120 °C.
Расплавление высокоуглеродистых материалов в зависимости от легирующих компонентов лежит в границах от 1100 до 1500 °C.
Точки плавления металлов и их сплавов находятся в очень широком температурном диапазоне, от очень низких температур (ртуть) до границы в несколько тысяч градусов
Знание этих показателей, а так же других физических свойств очень важно для людей, которые работают в металлургической сфере. Например, знание того, при какой температуре плавится золото и другие металлы пригодятся ювелирам, литейщикам и плавильщикам
Где производится бижутерия?
Есть несколько основных стран, которые могут похвастаться качеством своих изделий. Они доказывают, что бижутерия может выглядеть значительно лучше, чем золотые украшения.
- Италия – это лидер в производстве бижутерии. Украшения, которые там изготовляются, пользуются большой популярностью во всем мире. На острове Мурано производится муранское стекло, которое отличается своим необычным видом. Украшения производятся вручную лучшими итальянскими ювелирами. Такая бижутерия не является бюджетной.
- Франция. В этой стране есть несколько компаний, которые специализируются именно на изготовлении бижутерии.
- Чехия известна благодаря своим изделиям из граната. Ювелиры используют сплав «томпак», который не вызывает аллергию у человека.
- Бельгия отличается хорошим качеством украшений. Они служат долго своему хозяину и не темнеют.
Во избежание деформации необходимо снимать все украшения при большой активности, такой как бег или фитнес. Для продления срока жизни украшений лучше одевать их только на выход и снимать при выполнении домашних обязанностей.
Правильно подобранные ювелирные украшения способны подчеркнуть красоту и дополнить любой образ. Сейчас в моде массивные украшения из бижутерного сплава – это увесистые браслеты и подвески в геометрическом решении. Так же стоит присмотреться к новому тренду – броши. Они отличаются своим разнообразным видом и формой.
Общие сведения
Температурой плавления называют температуру, при которой твердое вещество переходит в жидкость. Медь расплавляется при температуре 1083 градусов, поэтому этот металл относят к категории тугоплавких. При снижении этой температуры металл может вновь принять твердую форму. Плавят медь на заводах, хотя эту процедуру можно провести в домашних условиях. На химическом уровне расплавление возникает за счет деструкции кристаллической решетки, которая формирует твердую структуру вещества. Атомы меди в кристаллической решетке всегда находятся в непрерывном движении.
Однако их взаимное притяжение и отталкивание происходит сбалансировано, поэтому атомы сохраняют исходное положение в течение длительного времени. В случае повышения температуры атомы меди получают дополнительную энергию, что заставляет двигаться их более интенсивно. При небольшом повышении дополнительная энергия «гасится» за счет сбалансированного движения атомов в решетке. Однако при достижении определенной температуры нагрева количество энергии становится избыточным, а кристаллическая решетка начинает разрушаться.
В этот момент и происходит расплавление вещества. Взаимное притяжение атомов частично сохраняется, поэтому вещество принимает жидкую форму. Однако в случае дальнейшего нагрева энергия атомов усиливается еще сильнее, что может привести к окончательному разрыву связи атомов друг с другом. Эту точку перехода называют испарением (жидкость трансформируется в пар). В случае снижения температуры медного пара может переходить обратно в жидкость, а потом — в твердое состояние.
Физические и химические параметры платины
Драгоценный химический элемент с атомным номером 78 представляет собой металл высокой плотности серого оттенка. В зависимости от угла освещения он может переливаться белым цветом. Металл обладает высокой пластичностью, инертностью к воздействию реагентов.
Платина была известна человечеству еще до нашей эры, ее использовали в Древнем Египте для изготовления украшений, дошедших до наших дней в форме артефактов. Племена инков применяли ее в качестве материала для изготовления изделий.
Но спустя много веков химический элемент был снова открыт, благодаря испанским путешественникам, которые осваивали Южную Америку. Даже название химического элемента происходит от испанского слова, обозначающего «маленькое серебро».
Поначалу платину принимали за «лунный металл», но в отличие от серебра температура ее плавления составляет 1772 °C. Со временем было обнаружено свойство металла: образовывать соединение с золотом. Этот факт повлек серию подделок монет и ювелирных изделий.
Драгоценный металл образует самородки, что обусловлено невысокой химической активностью. Основная добыча платины связана с месторождениями никелевых, медных руд. Основное производство платины (80%) сосредоточено в Южной Африке. Незначительное содержание металла в земной коре определяет объемы сырья на рынке.
У какого металла самая высокая температура плавления
 Вольфрам – самый тугоплавкий металл, 3422 °C (6170 °F).
Вольфрам – самый тугоплавкий металл, 3422 °C (6170 °F).
Твердый, тугоплавкий, достаточно тяжелый материал светло-серого цвета, который имеет металлический блеск. Механической обработке поддается с трудом. При комнатной температуре достаточно хрупок и ломается. Ломкость металла связана с загрязнением примесями углерода и кислорода.
Вольфрам можно получить из руды, благодаря сложным химическим переработкам, в качестве порошка. Используя прессование и спекание, из него создают детали обычной формы и бруски.
Вольфрам — крайне стойкий элемент к любым температурным воздействиям. По этой причине размягчить вольфрам не могли более сотни лет. Не существовало такой печи, которая смогла бы нагреться до нескольких тысяч градусов по Цельсию. Ученым удалось доказать, что это самый тугоплавкий металл. Хотя бытует мнение, что сиборгий, по некоторым теоретическим данным, имеет большую тугоплавкость, но это лишь предположение, поскольку он является радиоактивным элементом и у него небольшой срок существования.
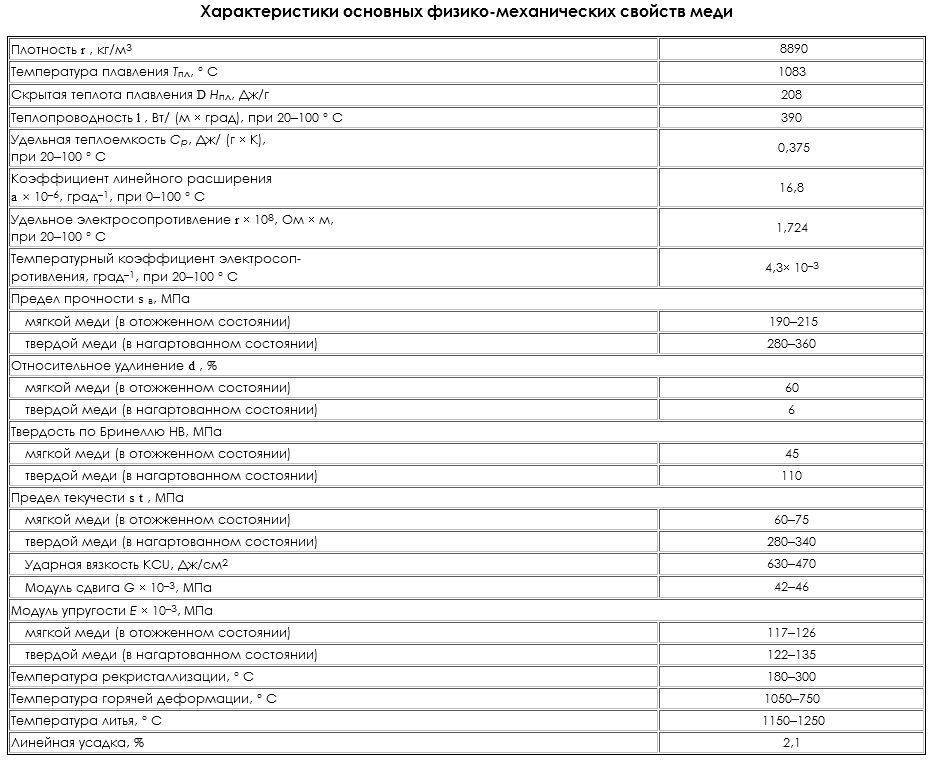
Физически свойства
Пластичный металл на открытом воздухе быстро покрывается оксидной пленкой, она и придает элементу характерный желтовато-красный оттенок, в просвете пленки могут иметь зеленовато-голубой цвет. Медь относится к тем немногим элементам, которые имеют заметную для глаза цветовую окраску. Она обладает высоким уровнем тепло- и электропроводности — это второе место после серебра.
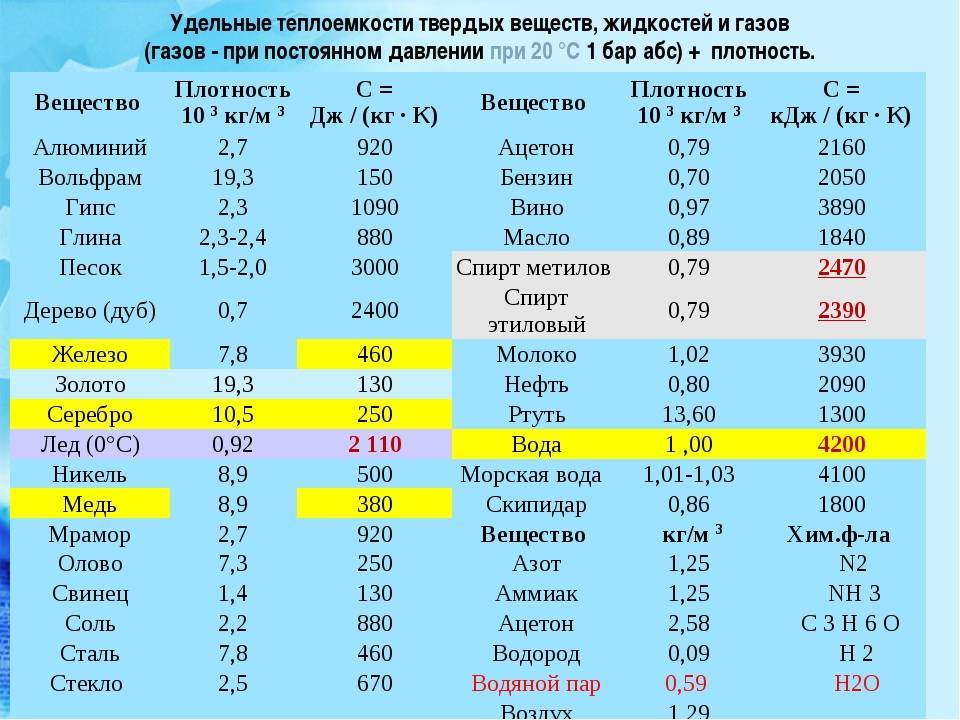
- Плотность — 8,94*103 кг/м3
- Удельная теплоемкость при Т=20оС — 390 Дж/кг*К
- Электрическое удельное сопротивление в температурном режиме от 20-100оС — 1,78*10-8Ом/м
- Температура кипения — 2595оС
- Удельная электропроводность при Т=20оС — 55,5-58 МСм/м.
Это интересно: Медная руда — месторождения, добыча, виды, переработка
При какой температуре плавится медь
Плавления происходит, когда из твердого состояния металл переходит в жидкое. Каждый элемент имеет собственную температуру плавления. Многое зависит от примесей в металле. Обычная температура плавления меди — 1083 ° C. Когда добавляется олово, температура снижается до 930- 1140 ° C. Температура плавления зависит здесь от содержания в сплаве олова. В сплаве купрума с цинком плавление происходит при 900- 1050 ° C .
При нагреве любого металла разрушается его кристаллическая решетка. По мере нагревания повышается температура плавления, но затем выравнивается по достижении определенного предела температуры. В этот момент и плавится металла. Полностью расплавляется, и температура повышается снова.
Когда металл охлаждается, температура снижается, в определенный момент остается на прежнем уровне, пока металл не затвердеет полностью. После полного затвердевания температура снижается опять. Это демонстрирует фазовая диаграмма, где отображен температурный процесс с начала плавления до затвердения. При нагревании разогретая медь при 2560 ° C начинает закипать. Кипение подобно кипению жидких веществ, когда выделяется газ и появляются пузырьки на поверхности. В момент кипения при максимально больших температурах начинается выделение углерода, образующегося при окислении.
Как удалить примеси в домашних условиях
Такая процедура также осуществима, но хочу обратить внимание на то, что работа с концентрированными кислотами требует предельной осторожности и должна проводиться в помещении с вентиляцией. Следующий этап – металлизация вещества. Хлорид серебра заливается соляной кислотой и осаждается при помощи мелкой цинковой стружки и нагревания
Полученный песок темно-серого цвета готов к переплавке
Хлорид серебра заливается соляной кислотой и осаждается при помощи мелкой цинковой стружки и нагревания. Полученный песок темно-серого цвета готов к переплавке
Следующий этап – металлизация вещества. Хлорид серебра заливается соляной кислотой и осаждается при помощи мелкой цинковой стружки и нагревания. Полученный песок темно-серого цвета готов к переплавке.
Как отличить медь от алюминия
Чистые металлы легко различить по цвету. Однако, довольно часто возникает необходимость идентифицировать луженую медь, имеющую серебристую окраску, или обогащенный медью алюминий, имеющий желтоватый цвет
Оба сплава используются для изготовления кабеля, а в некоторых случаях важно знать, из чего он сделан. В такой ситуации зрительный анализ не даст результата
Проще всего измерить сопротивление. У стометрового медного провода эта величина составляет 4 – 8 Ом, тогда как у алюминиевого – порядка 12 – 20 Ом. Достоинства такой методики в том, что кабель не повреждается.
Другой способ основан на разной прочности на изгиб. Если несколько раз согнуть и разогнуть алюминиевую жилу, она сломается, а медная выдержит такое испытание.
Наконец, можно подержать кабель в огне. Алюминий плавится уже при 600 град., медь — при значительно более высокой температуре. Необходимо понимать, что при нагревании, особенно на открытом огне, медь быстро покроется оксидной пленкой и изменит окраску. Этим можно пользоваться, чтобы отличить медь и от других сплавов.
Еще один универсальный способ — воздействие азотной кислотой. Аккуратно капните реактивом на изделие. Металлическая медь в зоне контакта окрасится в сине-зеленый цвет.
Дефицит меди.
Дефицит меди крайне редко встречается у людей. Основываясь на исследованиях, проводимых на животных и людях, последствия дефицита меди могут выражаться в: анемии, гиперхолестеринемии, нарушениях в соединительных тканях, остеопорозе и других дефектах кости, аномальном липидном обмене, атаксии и повышенном риске инфекций.
Люди с целиакией.
В исследовании 200 взрослых и детей с целиакией, из которых 69,9% утверждали, что придерживаются без глютеновой диеты, 15% имели дефицит меди (менее 70 мкг/дл в сыворотке у мальчиков и девочек моложе 12 лет и менее 80 мкг/дл у женщин старше 12 лет) в результате мельабсорбции кишечника и изменения слизистой оболочке кишечника, связанных с целиакией. В своих клинических руководствах по целиакии 2009 года Американский колледж гастроэнтерологии отмечает, что у людей с целиакией повышенный риск развития дефицита меди и что уровень меди нормализуется в течение месяца после начала адекватного приема меди с диетой без глютена.
Люди с болезнью Менкеса.
Менкеса — это редкое рецессивное нарушение гомеостаза меди. Нарушение клеточного транспорта меди, при котором наблюдается замедление роста, патологии нервной системы, судороги, характерное закручивание волос («болезнь курчавых волос»).
У этих людей кишечная абсорбция диетической меди резко падает, что приводит к признакам ее дефицита, в том числе к снижению уровня меди и ЦП в сыворотке крови.
Большинство людей с болезнью Менкеса умирают в возрасте 3 лет, если эту болезнь не лечить. Поэтому, детям с этим заболеваниям в первые несколько недель после рождения прописывают подкожные инъекции меди.
Люди, принимающие большие дозы препаратов с цинком.
Высокие дозы цинка в пище способны снижать усвоение меди, а употребление больших доз пищевых добавок цинка, может спровоцировать развитие дефицита меди. Имеются сведения о снижении содержания супероксиддисмутазы эритроцитов в меди и цинке, маркера статуса меди, даже при умеренно высоких дозах потребления цинка примерно 60 мг/день в течение 10 недель.
У людей, которые регулярно потребляют большие дозы цинка из добавок или используют чрезмерное количество цинксодержащих кремов для зубных протезов, может развиться дефицит меди, поскольку цинк может ингибировать абсорбцию меди.
Это одна из причин, по которой FNB установили ДВУ (UL) для цинка в количестве 40 мг/день для взрослых.