Маленький ликбез. О фотосинтезе.
Как известно, почти все вещества, из которых состоит любой живой организм (белки, жиры, углеводы, нуклеиновые кислоты, и т.д.) состоят на 99% всего из трёх химических элементов: углерода, кислорода и водорода. Оставшийся 1% составляют макроэлементы: азот, фосфор и калий, а также так называемые «микроэлементы» (прежде всего – железо, кальций, магний, цинк, в меньших количествах другие, — почти половина таблицы Менделеева). Зелёные растения обладают удивительным механизмом, позволяющим им самостоятельно синтезировать органические вещества из углекислого газа и воды. Под воздействием солнечного света особое вещество, содержащееся в их клетках – зелёный пигмент хлорофилл — производит из CO2 и H2O простой сахар – глюкозу, а уже из него, с помощью макро- и микроэлементов ферменты умеют делать белки, клетчатку, крахмал и всё остальное, что нужно для строительства растительного организма. В процессе этой реакции в окружающую среду выделяется кислород. Небольшую часть этого кислорода растения используют для дыхания, а остальное – выбрасывают в воздух или в воду.
Итак, для нормального роста и развития высших зелёных растений необходимо достаточное количество:
- углекислого газа;
- воды;
- солнечного света;
- макроэлементов (азот, фосфор, калий);
- микроэлементов (железо, кальций, магний, цинк, и др.)
Все эти компоненты должны быть сбалансированы друг с другом. Дефицит или избыток любого из них немедленно даёт преимущества не высшим растениям, а вредным паразитическим водорослям (зелёным нитчатым, багрянкам, диатомовым и другим), создающим в аквариуме проблемы. Эти организмы, которые старше цветковых растений на миллионы лет, приспособлены к любым условиям. Например, если в вашем аквариуме много света и мало СО2 – вы даёте преимущество нитчатым водорослям, способным быстро заполнить ваш аквариум спутанными волокнами тины. Что же делать, чтобы этого не произошло?
В химии и биохимии есть такое понятие – «лимитирующий фактор реакции». Что это такое – хорошо понятно тем, кто часто ходит в походы: скорость движения группы всегда равна скорости движения самого медленного из её участников, который и является «лимитирующим фактором». Так же точно и в росте аквариумных растений. Воды им хватает в избытке (они в ней живут!), макро- и микроэлементы поступают из грунта, из воды и с внесением удобрений, сделать хорошее яркое освещение – тоже не проблема, а вот с CO2 периодически возникают сложности. Он-то и становится в аквариуме «лимитирующим фактором». Почему? Почему проблемы с углекислотой возникают в аквариуме, но не возникают в природе? Давайте разберёмся…
Желудочно-кишечный тракт
Углекислый газ в организм попадает не только при дыхании, но и вместе с пищей. Углерод содержится практически во всех органических веществах, наибольшая концентрация содержится в продуктах растительного происхождения. Больше всего его образуется при расщеплении легкоусвояемых углеводов.
Углекислота влияет на химический состав жидкости в теле человека, хотя и не так значительно, но при сильном понижении или превышении может оказывать губительное воздействие. В организме почти все процессы жизнедеятельности клеток происходят при определенном уровне кислотно-щелочного баланса, который скорее близок к нейтральной воде, чем к кислоте. Наличие повышенной концентрации CO2 в употребляемых продуктах сильно меняет состав жидкости в теле человека. Это также влияет на протекание биохимических процессов. Происходит нарушение обмена веществ, гибель клеток или неправильный процесс их деления, что очень опасно.
Продукты и их кислотно-щелочной баланс
Поэтому продукты, содержащие CO2 в свободном состоянии (газировка) во многих странах запрещены к продаже.
Наибольший вред они наносят организму:
- При любых заболеваниях желудочно-кишечного тракта, в том числе хронических. Так как при приеме в пищу таких продуктов, происходит раздражение слизистой желудка. Они стимулируют выработку ферментов и повышают кислотность желудочного сока, что приводит к обострению имеющихся воспалительных процессов, образованию или углублению язвочек.
- Детям, до трех лет не стоит давать такие продукты, потому что их организм еще не совсем сформировался. Поэтому углекислота может привести к нарушению обмена веществ в организме и в будущем стать причиной высокой хрупкости костей.
- Диоксид углерода может вызвать аллергическую реакцию у человека.
- При наличии лишнего веса нельзя употреблять такие продукты, так как полнота, это следствие нарушения обмена веществ. А употребление продуктов с высоким содержанием CO2 приведет только к усугублению ситуации.
Во многих западных странах принят закон, в соответствии с которым наличие углекислого газа в продуктах не должно превышать 0,4%. Исключение дается только простой минеральной воде с газом, но только в том случае, если она содержит незначительное количество диоксида углерода. Но и это допустимо только по разрешению или рекомендации врача, особенно при болезнях желудка.
Что послушать
В новом эпизоде подкаста речь пойдет о том, что делать с ненужной одеждой, чем опасен текстиль на свалках и что такое свопы. Объем отходов модной индустрии в мире достигает 92 млн т в год, большая часть из них выбрасывается. На свалках одежда тлеет десятилетиями, выделяя метан и провоцируя пожары.
Чтобы этого избежать, необходимо перерабатывать ненужные вещи или отдавать их тем, кому они необходимы. О том, куда сдать текстиль, чтобы он не попал на свалку, расскажет Дарья Алексеева из фонда «Второе дыхание», который известен своими пунктами приема одежды и сетью магазинов Charity Shop.
Во второй части выпуска со-основательница проекта Swap it and never buy Наиля Гольман расскажет о свопах — еще одном способе подарить новую жизнь ненужным вещам.
Углекислый газ и мы: чем опасен CO2
Углекислый газ — один из продуктов обмена веществ в организме человека. Он играет большую роль в управлении дыханием и снабжением кровью органов. Рост содержания CO2 в крови вызывает расширение сосудов, способных таким образом транспортировать больше кислорода к тканям и органам. Аналогично и система дыхания понуждается к большей активности, если концентрация углекислоты в организме растет. Это свойство используют в аппаратах искусственной вентиляции легких, чтобы подстегнуть собственные органы дыхания пациента к большей активности.
https://youtube.com/watch?v=DqbvEhn5uJc
Кроме упомянутой пользы, превышение концентрации СO2 может принести организму и вред. Повышенное содержание во вдыхаемом воздухе приводит к тошноте, головной боли, удушью и даже к потере сознания. Организм протестует против углекислого газа и подает человеку сигналы. При дальнейшем увеличении концентрации развивается кислородное голодание, или гипоксия. Co2 мешает кислороду присоединяться к молекулам гемоглобина, которые и осуществляют перемещение связанных газов по кровеносной системе. Кислородное голодание ведет к снижению работоспособности, ослаблению реакции и способностей к анализу ситуации и принятию решений, апатии и может привести к смерти.
Общие симптомы отравления углекислым газом
Такие концентрации углекислого газа, к сожалению, достижимы не только в тесных шахтах, но и в плохо проветриваемых школьных классах, концертных залах, офисных помещениях и транспортных средствах — везде, где в замкнутом пространстве без достаточного воздухообмена с окружающей средой скапливается большое количество людей.
Где используется углекислый газ
Углекислый газ находится не только в теле человека и в окружающей атмосфере. Многие промышленные производства активно используют химическое вещество на различных стадиях технологических процессов. Его применяют в качестве:
- стабилизатора;
- катализатора;
- первичного или вторичного сырья.
Двуокись кислорода способствует преобразованию винограда во вкусное терпкое домашнее вино. При брожении сахара, содержащегося в ягодах, выделяется углекислый газ. Он придает напитку игристость, позволяет ощутить лопающиеся пузырьки во рту. На упаковке продуктов питания двуокись углерода скрывается под кодом Е290. Как правило, она используется в качестве консерванта для длительного хранения. При выпечке вкусных кексов или пирогов многие хозяйки добавляют в тесто разрыхлитель. В процессе приготовления образуются пузырьки воздуха, делающие сдобу пышной, мягкой. Это и есть углекислый газ — результат химической реакции между гидрокарбонатом натрия и пищевой кислотой. Любители аквариумных рыбок используют бесцветный газ в качестве активатора роста водных растений, а производители автоматических углекислотных установок помещают его в огнетушители.

«Одеяло Земли»
Углекислый газ (двуокись углерода, диоксид углерода, CO2) формируется при соединении двух элементов: углерода и кислорода. Он образуется в процессе сжигания угля или углеводородных соединений, при ферментации жидкостей, а также как продукт дыхания людей и животных. В небольших количествах он содержится и в атмосфере, откуда он ассимилируется растениями, которые, в свою очередь, производят кислород.
Углекислый газ бесцветен и тяжелее воздуха. Замерзает при температуре −78.5°C с образованием снега, состоящего из двуокиси углерода. В виде водного раствора он образует угольную кислоту, однако она не обладает достаточной стабильностью для того, чтобы ее можно было легко изолировать.
Углекислый газ — это «одеяло» Земли. Он легко пропускает ультрафиолетовые лучи, которые обогревают нашу планету, и отражает инфракрасные, излучаемые с ее поверхности в космическое пространство. И если вдруг углекислый газ исчезнет из атмосферы, то это в первую очередь скажется на климате. На Земле станет гораздо прохладнее, дожди будут выпадать очень редко. К чему это в конце концов приведет, догадаться нетрудно.
Правда, такая катастрофа нам пока еще не грозит. Скорее даже, наоборот. Сжигание органических веществ: нефти, угля, природного газа, древесины – постепенно увеличивает содержание углекислого газа в атмосфере. Значит, со временем надо ждать значительного потепления и увлажнения земного климата. Кстати, старожилы считают, что уже сейчас заметно теплее, чем было во времена их молодости…
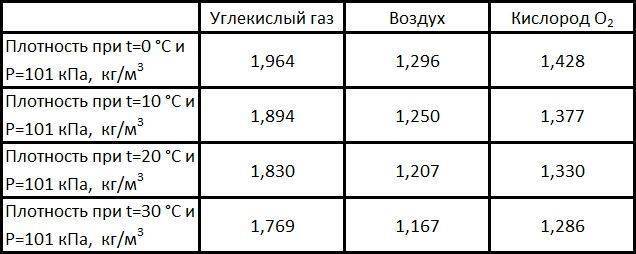
Двуокись углерода выпускается жидкая низкотемпературная, жидкая высокого давления и газообразная. Ее получают из отбросных газов производств аммиака, спиртов, а также на базе специального сжигания топлива и других производств. Газообразная двуокись углерода – газ без цвета и запаха при температуре 20°С и давлении 101,3 кПа (760 мм рт. ст.), плотность – 1,839 кг/м3. Жидкая двуокись углерода – просто бесцветная жидкость без запаха.
Углекислый газ нетоксичен и невзрывоопасен. При концентрациях более 5% (92 г/м3) двуокись углерода оказывает вредное влияние на здоровье человека — она тяжелее воздуха и может накапливаться в слабо проветриваемых помещениях у пола. При этом снижается объемная доля кислорода в воздухе, что может вызвать явление кислородной недостаточности и удушья.
Тема недели: Что делать с CO2
Глобальный переход на экологически чистые виды энергии займет не один год, а снизить выбросы парниковых газов необходимо уже сейчас. В этом может помочь технология улавливания углекислого газа.
Способ придумали достаточно давно: первый завод, который начал работать с этой технологией, построили в США в 1972 году. По данным исследовательского центра Global CCS Institute за 2019 год, в мире работает всего 19 предприятий, которые улавливают CO2, еще 32 находятся на разных стадиях строительства. Их так мало потому что подобные проекты стоили очень дорого.
Благодаря научно-техническому прогрессу сегодня эта технология стала более доступной, и в мире ее начинают применять более масштабно. Например, правительство Норвегии планирует потратить $2,6 млрд на развитие программы «Northern Lights». В первую очередь проект затронет мусоросжигающие заводы и цементные фабрики, потому что их производственный цикл сложно сделать более экологичным. CO2, который выбрасывают эти предприятия, планируют собирать и сжижать. После этого углекислый газ будут «закапывать» на морском дне — например, по трубам отправлять в отработанные нефтяные месторождения. Там он вступит в реакцию с минералами и осадочными породами и в форме карбоната сможет тысячи лет оставаться на морском дне.
Ученые из проекта «Веста» (Project Vesta) тоже предлагают хранить углекислый газ в океанах. Они хотят связывать CO2 при помощи химических реакций, распространенных в природе. Дождевая вода, которая содержит в себе углекислый газ, особенно сильно взаимодействует с минералами, богатыми кремнием, кальцием и магнием. Продукты этих реакций затем попадают в океан, а морские организмы перерабатывают их и строят свои панцири. В естественной среде такой процесс длится долго, и ученые хотят его ускорить. Они предлагают делать пляжи из оливина — минерала, который содержит магний и кремний и легко разрушается. Так продукты химической реакции будут попадать в море быстрее, а значит, получится собрать больше CO2. При этом участники проекта указывают на низкую стоимость решения — 1 т углекислого газа можно переработать всего за $10.
Как , CO2 способен принести пользу в разных сферах промышленности. Так, с помощью углекислого газа можно эффективнее добывать нефть, а также производить из него бетонные блоки для строительства и создавать новые виды топлива, материалов и удобрений. В результате уровень выбросов CO2 может не только снизиться до нуля, но и стать отрицательным.
Нахождение в природе[ | ]
Основная статья: Геохимический цикл углерода
Углекислый газ содержится в атмосфере, гидросфере, литосфере и биосфере. Обмен углерода между ними происходит в основном за счёт двуокиси углерода. В 2020 году в атмосфере содержалось примерно около 830 гигатонн (830 миллиардов тонн) углерода в форме двуокиси углерода. Гидросфера содержит около 38 000 гигатонн углерода в виде физически растворенного диоксида углерода, а также растворенных гидрокарбонатов и карбонатов. Литосфера содержит самую большую долю химически связанного диоксида углерода. Карбонатные породы, такие как кальцит и доломит, содержат около 60 000 000 гигатонн углерода. Кроме того, большие количества углерода хранятся в районах вечной мерзлоты, таких как тундры арктических и полярных антарктических регионов, в бореальных хвойных лесах или высоких горах и на болотах.
Химические свойства углекислого газа. Химические реакции (уравнения) углекислого газа:
Диоксид углерода относится к кислотным оксидам, поэтому для него характерны следующие химические реакции:
1. реакция взаимодействия оксида углерода (IV) и водорода:
CO2 + 4H2 → CH4 + 2H2O (t ~ 200 °C, kat = Cu2O).
В результате реакции образуются метан и вода.
2. реакция взаимодействия оксида углерода (IV) и углерода:
CO2 + C ⇄ 2CO (t = 700-1000 °C).
В результате реакции образуется оксид углерода (II). Реакция протекает при взаимодействии углекислого газа с раскаленными углями.
3. реакция взаимодействия оксида углерода (IV) и магния:
CO2 + 2Mg → 2MgO + C (t ~ 500 °C).
В результате реакции образуются оксид магния и углерод.
4. реакция взаимодействия оксида углерода (IV) и гафния:
Hf + CO2 → HfC + HfO2 (t = 800-1000 °C).
В результате реакции образуются карбид гафния и оксид гафния.
5. реакция взаимодействия оксида углерода (IV) и германия:
Ge + CO2 → GeO + CO (t = 700-900 °C).
В результате реакции образуются оксид германия и оксид углерода (II).
6. реакция взаимодействия оксида углерода (IV) и цинка:
Zn + CO2 → ZnO + CO (t = 800-950 °C).
В результате реакции образуются оксид цинка и оксид углерода (II).
7. реакция взаимодействия оксида углерода (IV) и индия:
2In + CO2 → In2O + CO (t ~ 850 °C).
В результате реакции образуются оксид индия и оксид углерода (II).
8. реакция взаимодействия оксида углерода (IV) и циркония:
2Zr + CO2 → ZrC + ZrO2 (t = 800-100 °C).
В результате реакции образуются карбид циркония и оксид циркония.
9. реакция взаимодействия оксида углерода (IV) и вольфрама:
W + 2CO2 → WO2 + 2CO (t ~ 1200 °C).
В результате реакции образуются оксид вольфрама и оксид углерода (II).
10. реакция взаимодействия оксида углерода (IV) и оксида лития:
Li2O + CO2 → Li2CO3.
В результате реакции образуется карбонат лития.
11. реакция взаимодействия оксида углерода (IV) и оксида натрия:
Na2O + CO2 → Na2CO3 (t = 450-550 °C).
В результате реакции образуется карбонат натрия.
12. реакция взаимодействия оксида углерода (IV) и оксида калия:
K2O + CO2 → K2CO3 (t ~ 400 °C).
В результате реакции образуется карбонат калия.
13. реакция взаимодействия оксида углерода (IV) и оксида бария:
BaO + CO2 → BaCO3.
В результате реакции образуется карбонат бария.
14. реакция взаимодействия оксида углерода (IV) и оксида кальция:
CaO + CO2 → CaCO3.
В результате реакции образуется карбонат кальция.
15. реакция взаимодействия карбоната кальция, оксида углерода (IV) и воды:
CaCO3 + CO2 + H2O → Ca(HCO3)2.
В результате реакции образуется гидрокарбонат кальция.
16. реакция взаимодействия оксида углерода (IV) и оксида магния:
MgO + CO2 → MgCO3.
В результате реакции образуется карбонат магния.
17. реакция взаимодействия оксида углерода (IV) и оксида кремния (II):
SiO + CO2 → SiO2 + CO (t ~ 500 °C).
В результате реакции образуются оксид кремния (IV) и оксид углерода (II).
18. реакция взаимодействия оксида углерода (IV) и воды:
CO2 + H2O ⇄ H2CO3.
В результате реакции образуется угольная кислота.
19. реакция взаимодействия оксида углерода (IV) и гидроксида лития:
2LiOH + CO2 → Li2CO3 + H2O.
В результате реакции образуются карбонат лития и вода. В ходе реакции используется концентрированный раствор гидроксида лития.
20. реакция взаимодействия оксида углерода (IV) и гидроксида калия:
KOH + CO2 → KHCO3,
2KOH + CO2 → K2CO3 + H2O.
В первом случае в результате реакции образуются гидрокарбонат калия, во втором случае – карбонат калия и вода. Реакция протекает в первом случае в этаноле и используется разбавленный раствор гидроксида калия, во втором используется концентрированный раствор гидроксида калия.
21. реакция взаимодействия оксида углерода (IV) и гидроксида натрия:
NaOH + CO2 → NaHCO3,
2NaOH + CO2 → Na2CO3 + H2O.
В первом случае в результате реакции образуются гидрокарбонат натрия, во втором – карбонат натрия и вода. В ходе первой реакции используется разбавленный раствор гидроксида натрия, в ходе второй – концентрированный раствор гидроксида натрия.
22. реакция взаимодействия оксида углерода (IV) и гидроксида кальция:
Ca(OH)2 + CO2 → CaCO3 + H2O.
В результате реакции образуются карбонат кальция и вода.
23. реакция взаимодействия оксида углерода (IV) и гидроксида бария:
Ba(OH)2 + CO2 → BaCO3 + H2O.
В результате реакции образуются карбонат бария и вода.
24. реакция взаимодействия оксида углерода (IV) и метана:
CH4 + CO2 → 2CO + 2H2 (t = 800-900 °C, kat = NiO, нанесенный на Al2O3).
В результате реакции образуются оксид углерода (II) и вода.
25. реакция термического разложения оксида углерода (IV):
2CO2 → 2CO + O2 (t > 2000 °C).
В результате реакции образуются оксид углерода (II) и кислород.
26. реакция фотосинтеза:
6CO2 + 6H2O → C6H12O6 + 6O2 (hv, kat = хлорофилл).
В результате реакции образуются глюкоза и кислород.
Применение
В пищевой промышленности углекислота используется как консервант и разрыхлитель, обозначается на упаковке кодом Е290.
В криохирургии используется как одно из основных веществ для криоабляции новообразований.
Жидкая углекислота широко применяется в системах пожаротушения и в огнетушителях. Автоматические углекислотные установки для пожаротушения различаются по системам пуска, которые бывают пневматическими, механическими или электрическими.
Устройство для подачи углекислого газа в аквариум может включать в себя резервуар с газом. Простейший и наиболее распространенный метод получения углекислого газа основан на конструкции для изготовления алкогольного напитка браги. При брожении, выделяемый углекислый газ вполне может обеспечить подкормку аквариумных растений
Углекислый газ используется для газирования лимонада и газированной воды. Углекислый газ используется также в качестве защитной среды при сварке проволокой, но при высоких температурах происходит его распад с выделением кислорода. Выделяющийся кислород окисляет металл. В связи с этим приходится в сварочную проволоку вводить раскислители, такие как марганец и кремний. Другим следствием влияния кислорода, также связанного с окислением, является резкое снижение поверхностного натяжения, что приводит, среди прочего, к более интенсивному разбрызгиванию металла, чем при сварке в инертной среде.
Углекислота в баллончиках применяется в пневматическом оружии (в газобаллонной пневматике) и в качестве источника энергии для двигателей в авиамоделировании.
Хранение углекислоты в стальном баллоне в сжиженном состоянии выгоднее, чем в виде газа. Углекислота имеет сравнительно низкую критическую температуру +31 °С. В стандартный 40-литровый баллон заливают около 30 кг сжиженного углекислого газа, и при комнатной температуре в баллоне будет находиться жидкая фаза, а давление составит примерно 6 МПа (60 кгс/см²). Если температура будет выше +31 °С, то углекислота перейдёт в сверхкритическое состояние с давлением выше 7,36 МПа. Стандартное рабочее давление для обычного 40-литрового баллона составляет 15 МПа (150 кгс/см²), однако он должен безопасно выдерживать давление в 1,5 раза выше, то есть 22,5 МПа, — таким образом, работа с подобными баллонами может считаться вполне безопасной.
Твёрдая углекислота — «сухой лёд» — используется в качестве хладагента в лабораторных исследованиях, в розничной торговле, при ремонте оборудования (например: охлаждение одной из сопрягаемых деталей при посадке внатяг) и т. д. Для сжижения углекислого газа и получения сухого льда применяются углекислотные установки.
Откуда же появляется углекислый газ?
Почва
Данный вид газа активно образуется в результате химических процессов в толще Земли. Он способен выходить через трещины и разломы в земной коре, что представляет большую опасность для работников шахт горнодобывающей промышленности. Как правило, в шахтном воздухе углекислый газ присутствует практически всегда в повышенном количестве.
В некоторых видах горных выработок, например, на угольных и калийных месторождениях, газ способен накапливаться с большой скоростью. Повышенная концентрация приводит к ухудшению самочувствия и удушению, поэтому максимальное значение не должно превышать 1% от общего объема воздуха в шахте.
Промышленность и транспорт
Одним из крупнейших источников образования углекислого газа являются различные заводы. Промышленные предприятия в ходе выполнения технологических процессов вырабатывают его в огромном количестве, выбрасывая в атмосферу. Такое же влияние оказывает транспорт. В богатом составе выхлопных газов имеется также и углекислый газ. При этом большую долю его выбросов в атмосферу планеты вносят самолеты. На втором месте идет наземный транспорт. Наибольшая концентрация создается над крупным городами, которым присущи не только большое количество автомобилей, но и затяжные «пробки».
Дыхание
Практически все живые существа планеты, при выдыхании выделяют углекислый газ. Он образуется в результате химических обменных процессов в легких и тканях. Это количество в масштабах планеты, даже с учетом миллиардов существ, весьма незначительно. Однако есть обстоятельства, когда о выделении углекислого газа с дыханием необходимо помнить.
В первую очередь, это замкнутые пространства, комнаты, аудитории, лифты и т.д. При скоплении достаточного количества людей на ограниченной территории достаточно быстро наступает духота. Она является недостатком кислорода из-за того, что он замещается выдыхаемым углекислым газом, который непригоден для дыхания. Чтобы избежать этого, необходимо осуществлять естественную или принудительную вентиляцию, с целью введения в помещение нового воздуха с улицы. Вентилирование помещений может производиться как при помощи обычных форточек, так и сложных систем с системой воздуховодов и нагнетающими турбинами.
Причины образования инея на баллоне
Постараемся разобраться, почему происходит так, что замерзает газ в баллоне, находящемся на улице, при понижении температуры воздуха. Так, для начала нужно понять, что охлаждение частиц происходит при интенсивном высвобождении газа из баллона. Поскольку газ внутри емкости закачивается под давлением, он сконцентрирован в жидком состоянии. Вследствие этого происходит частичное замерзание жидкого газа во время его высвобождения.
Причина первая — низкая температура воздуха
Исходя из практики использования баллонов, оптимальная температура при которой оборудование будет нормально работать составляет примерно 10 градусов, а при снижении этой отметки, начинаются проблемы с подачей газа в систему.
Если ваше оборудование находится в помещении с отоплением, тогда не стоит обращать внимание на эти показатели. Также не стоит беспокоиться о том, что ваш газовый баллон замерзнет и выйдет из строя, если оставить его в помещении без отопления в зимнюю пору года
Зимняя температура слишком маленькая, чтобы полностью заморозить топливо.
Причина вторая — высокое содержание бутана
А сейчас разберемся, может ли замерзнуть газ, который находится внутри баллона, и как это предотвратить. Так, чтобы обеспечить правильную работу газовых приборов, необходимо соблюдать правильное соотношение пропана и бутана. Правильные пропорции помогут достичь максимального потребления топлива и корректной работы приборов при отрицательной температуре окружающей среды.
Пропорции топлива летом
Как уже было сказано раньше, температура замерзания бутана, отличается от граничной температуры замерзания пропана. Путём практических исследований были выведены оптимальные пропорции для работы оборудования зимой и летом.
Для теплого времени года, топливо смешивается в таких пропорциях:
- Пропан – 40 %;
- Бутан 60 %.
Такое соотношение считается наиболее эффективным для потребления. Стоит отметить, что этот вариант имеет более низкую стоимость, чем топливо с «зимней» пропорцией.
Зимние пропорции топлива
Для использования газовых баллонов зимой пропорции будут другими, а именно:
- Пропан – 60 %;
- Бутан – 40 %.
В некоторых случаях количество пропана может достигать 80 процентов. Но, исходя из того, что пропан стоит дороже, чем бутан, итоговая цена на топливо также будет выше.
Причина третья — повышенное потребление газа
Но всё же, почему емкость покрывается инеем только в том месте, где газ находится в жидком состоянии? Низкая температура окружающей среды – не единственная причина обмерзания. Как известно, газовая плита, камин или другое оборудование, которое работает от газового баллона, функционирует при преобразовании газа из жидкого состояния в парообразный вид.
Есть два варианта преобразования газа, а именно:
- нагревание топлива;
- естественное испарение.
В этом случае все частицы с мощной кинетической энергией стремительно направляются в верхнюю часть емкости и отделяются от частиц в жидком состоянии с меньшим кинетическим потенциалом.
Газ, который пребывает в жидком состоянии внутри баллона, всегда находится внизу, а паровая часть стремится вверх. Таким образом и осуществляется высвобождение топлива и подача его в газовую плиту или другое оборудование
В связи с такими условиями жидкое топливо начинает терять температуру. Из этого следует, что при повышении потребления газа понижается температура его жидкого состояния. Проще говоря, чем больше топлива потребляет оборудование, тем быстрее будет замерзать газовый баллон.
По мере охлаждения частиц понижается способность самостоятельного испарения сжиженного газа. Отсюда следует, чем холоднее будут частицы, тем медленнее будет испаряться газ. При этом оборудование начинает работать с перебоями или вовсе перестаёт функционировать.
Углекислый газ, формула, молекула, строение, состав, вещество:
Углекислый газ (диоксид углерода, двуокись углерода, углекислота, оксид углерода (IV), угольный ангидрид) – бесцветный газ, почти без запаха (в больших концентрациях с кисловатым «содовым» запахом).
Углекислый газ – бинарное химическое соединение углерода и кислорода, имеющее формулу CO2.
Химическая формула углекислого газа CO2.
Строение молекулы углекислого газа, структурная формула углекислого газа:
Углекислый газ тяжелее воздуха приблизительно в 1,5 раза. Его плотность при нормальных условиях составляет 1,98 кг/м3, по отношении к воздуху – 1,524. Поэтому скапливается в низких непроветриваемых местах.
Концентрация углекислого газа в воздухе (в атмосфере Земли) составляет в среднем 0,046 % (по массе) и 0,0314 % (по объему).
Углекислый газ вырабатывается в органах и тканях человека образуется в качестве одного из конечных продуктов метаболизма. Он переносится от тканей по венозной системе и затем выделяется с выдыхаемым воздухом через лёгкие. Таким образом, содержание углекислого газа в крови велико в венозной системе, уменьшается в капиллярной сети лёгких, и содержание его мало в артериальной крови. В выдыхаемом человеком воздухе содержится около 4,5% диоксида углерода, что в 60-110 раз больше, чем во вдыхаемом. Организм человека выделяет приблизительно 1 кг углекислого газа в сутки.
Углекислый газ растворяется в воде. В 100 граммах воды растворяется 0,3803 грамма CO2 при 16 °C, 0,3369 грамма CO2 – при 20 °C, 0,2515 грамма CO2 – при 30 °C. Растворяясь в воде, образует угольную кислоту Н2CO3. Растворим также в ацетоне, бензоле, метаноле и этаноле.
Термически устойчив при температурах менее 1000 °C. При температуре 1000 °C восстанавливается углем до оксида углерода (II).
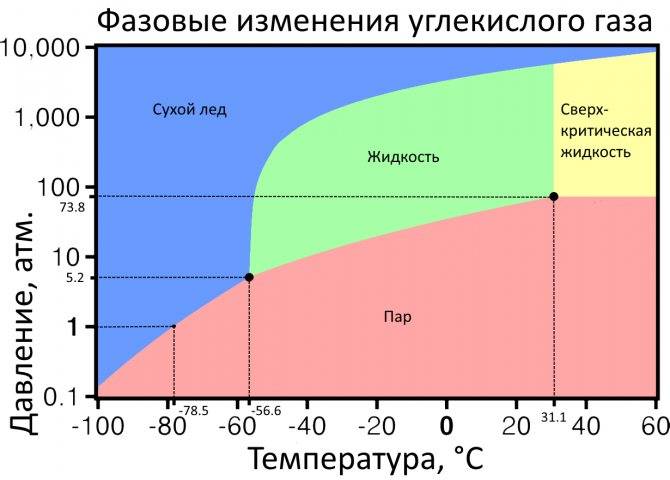
При нормальном атмосферном давлении диоксид углерода не существует в жидком состоянии, существует только в твердом или газообразном состоянии. Твердая двуокись углерода при повышении температуры не плавится, а переходит (возгоняется) непосредственно из твёрдого состояния в газообразное. Твёрдую двуокись углерода также называют сухим льдом. Внешний вид сухого льда напоминает обычный лед, снегоподобную массу. При сублимации сухой лед поглощает около 590 кДж/кг (140 ккал/кг) теплоты.
Под давлением 35 000 атм. твердая углекислота становится проводником электрического тока.
Жидкий углекислый газ можно получить при повышении давления. Так, при температуре 20 °С и давлении свыше 6 МПа (~60 атм.) газ сгущается в бесцветную жидкость. При нормальных условиях (20 °С и 101,3 кПа) при испарении 1 кг жидкой углекислоты образуется 509 л углекислого газа. Хранят и транспортируют углекислый газ, как правило, в жидком состоянии
Двуокись углерода негорюча, но в ее атмосфере может поддерживаться горение активных металлов, например, щелочных металлов и щелочноземельных – магния, кальция, бария.
Двуокись углерода нетоксична, невзрывоопасна.
Предельно допустимая концентрация двуокиси углерода в воздухе рабочей зоны не установлена, при оценке этой концентрации можно ориентироваться на нормативы для угольных и озокеритовых шахт, установленные в пределах 0,5% (об.) или 9,2 г/м (см. ГОСТ 8050-85 «Двуокись углерода газообразная и жидкая. Технические условия»).
По степени воздействия на организм человека двуокись углерода относится к 4-му классу опасности по ГОСТ 12.1.007-76.
При концентрациях более 5% (92 г/м) двуокись углерода оказывает вредное влияние на здоровье человека, так как она тяжелее воздуха в полтора раза и может накапливаться в слабопроветриваемых помещениях у пола и в приямках, а также во внутренних объемах оборудования для получения, хранения и транспортирования газообразной, жидкой и твердой двуокиси углерода. При этом снижается объемная доля кислорода в воздухе, что может вызвать явление кислородной недостаточности и удушья.
Углекислый газ образуется при гниении и горении органических веществ, в результате вулканической деятельности. Содержится в воздухе и минеральных источниках, выделяется при дыхании животных и растений. Искусственными источниками образования углекислого газа являются промышленные выбросы и выхлопные газы автомобильного транспорта.
Углекислый газ легко пропускает излучение в ультрафиолетовой и видимой частях спектра, которое поступает на Землю от Солнца и обогревает её. В то же время он поглощает испускаемое Землёй инфракрасное излучение и является одним из парниковых газов, вследствие чего участвует в процессе глобального потепления.
Почему CO2 в аквариуме – дефицит?
Посмотрите на биотоп любого природного пресного водоёма. Водных растений там обычно немного, и сидят они редко, а дно покрыто органическими отложениями, в которых в изобилии живут разнообразные микро- и макроорганизмы, в основном беспозвоночные. Да и рыбы изрядно, и головастиков… И все они – от микроорганизмов, перерабатывающих донные отложения, до рыбы и лягушек, выделяют в воду значительные количества СО2. Иное дело – типичный растительный аквариум, который, как правило, густо засажен растениями, а рыбы в нём мало, и она невелика (ибо большинство крупных рыб портят растения). Обычное население наших аквариумов – мелкая стайная харацинка и гуппи с пецилиями, которые в силу малого размера и медленного обмена веществ углекислого газа выделяют совсем мало.
А вот света в наших обычных аквариумах в достатке, азота с фосфором – обычно тоже хватает. Вот и получается, что тем самым «лимитирующим фактором» становится СО2. Часть растений при его дефиците просто угнетаются в росте и в конце концов погибает, а другие – приспособились сами добывать себе СО2 из минеральных веществ, разлагая растворённые в любой воде гидрокарбонаты. При этом в качестве «побочного продукта» образуются нерастворимые соли кальция, выпадающие на листьях таких растений в виде грубой некрасивой корки (на которой быстро поселяются одноклеточные диатомовые водоросли). Такой фокус умеют проделывать элодеи, анубиасы, роголистники и некоторые другие виды, живущие в природе в стоячих водоёмах и сталкивающиеся там с периодическим дефицитом углекислоты. Так что если мы хотим, чтобы растения выглядели так, как на картинках в интернете, а не являли из себя тощие унылые и понурые хвостики, покрытые известковой коркой и водорослевыми обрастаниями, то волей-неволей придётся подумать о добавлении в аквариум углекислого газа.
Если же вы привыкли более дотошно подходить к таким проблемам, и мои краткие пояснения вас не убедили — советую обратиться к научной статье вот по этой ссылке, в которой всё это подробно разъяснено с точки зрения химии и биохимии:
- Углекислый газ и карбонатная система воды. Часть 1.
- Углекислый газ и карбонатная система воды. Часть 2.
Мы же перейдём к практике. Но прежде — маленькое предупреждение: